Gli esperti esaminano i protocolli degli studi clinici prima di avviare gli studi per assicurarsi che siano basati su una solida scienza. Tutti gli studi clinici finanziati dal governo federale devono passare attraverso questo tipo di revisione.Molti altri sponsor di sperimentazioni cliniche, come le aziende farmaceutiche, cercano anche la consulenza di esperti sul merito scientifico dei loro protocolli di sperimentazione.
Commissioni di revisione istituzionale (IRB)
Queste commissioni esaminano anche i protocolli degli studi clinici prima che gli studi possano iniziare. I membri del consiglio si assicurano che il rischio di danni in un processo sia basso e che gli eventuali danni siano ragionevoli rispetto ai possibili benefici. Osservano inoltre da vicino i progressi in corso della sperimentazione dall'inizio alla fine e devono riesaminare le prove in corso almeno una volta all'anno. Gli IRB possono richiedere modifiche al protocollo o persino interrompere la sperimentazione, se necessario per garantire la sicurezza del paziente.
Le regole federali richiedono che ogni IRB includa almeno cinque persone. Deve includere:
- uno scienziato
- una persona che non è uno scienziato
- una persona che non è associata all'istituzione in cui si svolge il processo e che non è un familiare diretto di qualcuno che è associato a tale istituzione
Gli IRB possono anche includere medici, infermieri, assistenti sociali, cappellani, avvocati dei pazienti e altri professionisti sanitari o comunitari. Tutti i membri di un IRB devono essere istruiti sullo scopo, le funzioni e le responsabilità dell'IRB, come indicato nelle normative federali.
Nella maggior parte dei casi, gli IRB si trovano dove si svolgerà il processo. Molte istituzioni che conducono studi clinici hanno i propri IRB. Una sperimentazione clinica che si svolge in più di un istituto viene spesso sottoposta a revisione da parte dell'IRB di ciascuna istituzione.
Schede di monitoraggio dei dati e della sicurezza (DSMB)
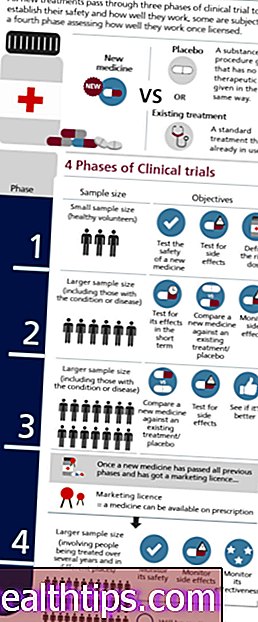
Alcuni studi clinici, in particolare gli studi clinici di fase III, che spesso coinvolgono molte istituzioni, utilizzano un DSMB. Analogamente agli IRB, i DSMB esaminano i progressi di una sperimentazione clinica e monitorano la sicurezza dei partecipanti. Esaminano anche i dati sull'efficacia degli interventi di prova. Ogni prova ha un solo DSMB.
Un DSMB è un gruppo di medici, statistici e altri che sono indipendenti dalle persone, dalle organizzazioni e dalle istituzioni che sponsorizzano, organizzano e conducono la sperimentazione clinica. I membri del DSMB sono esperti nella ricerca clinica e nelle sperimentazioni cliniche. Garantiscono che i dati della sperimentazione siano completi e possono interrompere una sperimentazione in anticipo se sorgono problemi di sicurezza o se si ottiene una risposta alla domanda principale della ricerca prima del previsto. Interrompere anticipatamente una sperimentazione perché è stata data risposta alla domanda principale della ricerca può consentire alle persone che non partecipano alla sperimentazione di accedere prima a un intervento efficace. I DSMB hanno programmato riunioni per esaminare i dati clinici e i loro verbali o raccomandazioni delle riunioni vengono inoltrati agli IRB.
Ufficio per la protezione della ricerca umana (OHRP)
Questo ufficio protegge le persone che prendono parte alla ricerca e fornisce la leadership a molte agenzie federali che svolgono ricerche coinvolgendo le persone.
L'OHRP applica importanti normative per la protezione dei pazienti negli studi clinici, chiamate Regola Comune. Questi regolamenti definiscono gli standard riguardanti:
- il processo di consenso informato
- Formazione e funzione dell'IRB
- il coinvolgimento di detenuti, bambini e altri gruppi vulnerabili nella ricerca
Food and Drug Administration (FDA)
La FDA svolge anche un ruolo nella protezione delle persone che prendono parte alla ricerca e nel garantire l'integrità dei dati delle sperimentazioni. La FDA può rimuovere i ricercatori dalla conduzione di studi clinici quando il ricercatore ha ripetutamente o intenzionalmente non seguito le regole intese a proteggere i pazienti. O quando il ricercatore non ha garantito l'integrità dei dati. La FDA approva i nuovi farmaci prima che possano essere venduti. Questo aiuta:
- prevenire ciarlatani
- assicurarsi che i farmaci funzionino come dovrebbero
- assicurati che i benefici per la salute del farmaco superino i loro rischi
Riprodotto con il permesso del National Cancer Institute del NIH. NIH non avalla né consiglia alcun prodotto, servizio o informazione qui descritto o offerto da Healthline. Ultima revisione della pagina il 22 giugno 2016.



.jpg)